Мужское бесплодие
Уникальный 15-летний опыт работы в НИИ им. Д.О. Отта руководителя клиники доцента Игнатовского А.В.
Современные протоколы обследования и лечения пациентов с диагнозом мужское бесплодие.
Мужское бесплодие является актуальной проблемой и приобретает особую медицинскую и социальную значимость как у нас в стране, так и за рубежом. Это связано с увеличением частоты заболеваний половых органов у мужчин, ростом аномалий развития, обусловленных влиянием вредных факторов внешней среды, аллергизацией населения, широким и бесконтрольным применением лекарственных средств и другими факторами. Нарушение фертильности приводит к росту бесплодных браков, разводов и ухудшению демографических показателей. Удельный вес бесплодных браков в мире достигает 15%, причем половина из них обусловлена бесплодием мужчин.
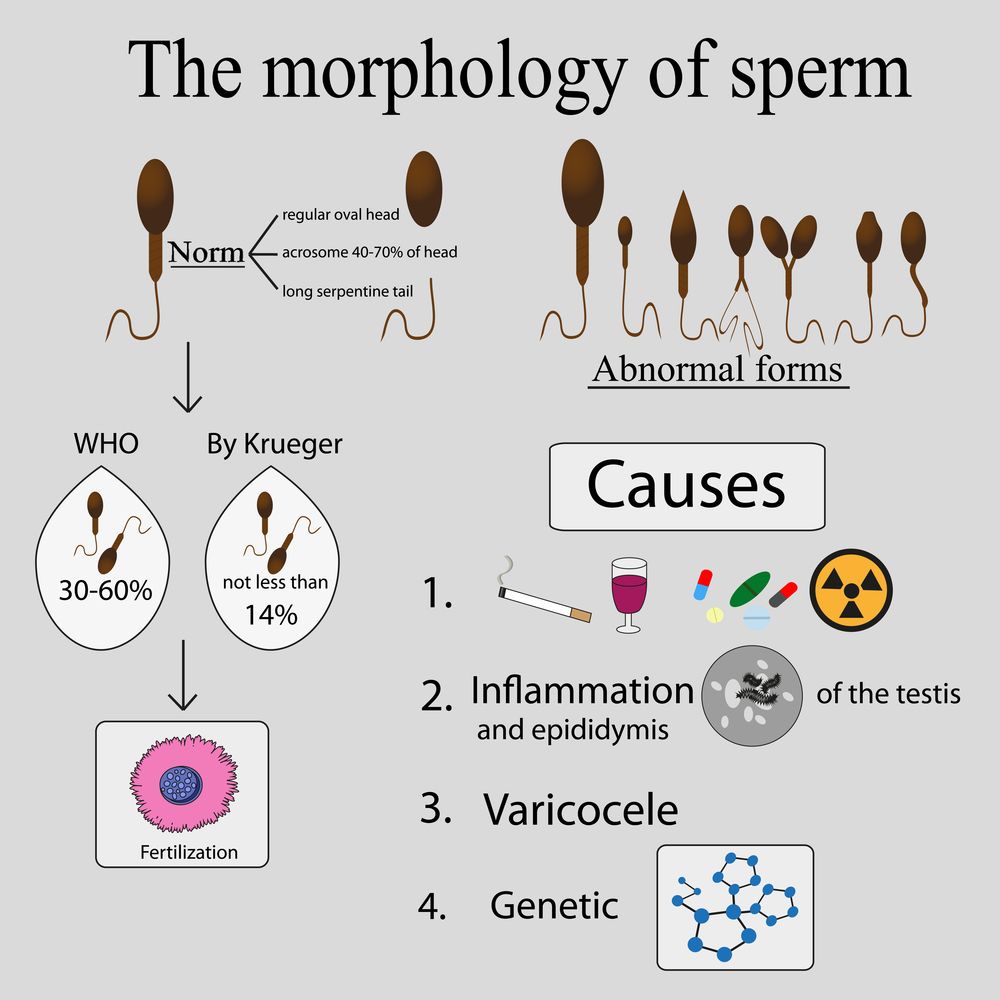
Причины мужского бесплодия
Бесплодие мужчин возникает в результате многочисленных патологических процессов в организме, которые вызывают дистрофические изменения в семенных канальцах и межуточной ткани яичек, приводя к развитию патоспермии (изменения в эякуляте) и нарушению секреции половых гормонов.
Нервно-психический фактор мужского бесплодия
В большинстве случаев ЦНС первой среди других систем организма реагирует, обеспечивая существенные изменения метаболизма. Это происходит чаще всего с участием промежуточных звеньев гипоталамуса и гипофиза.
Тяжелая психическая травма, воздействуя через половой центр гипоталамуса, нередко приводит к олиго- или азооспермии.
Серьезные повреждения сперматогенного эпителия яичек, возникающие при травме спинного мозга, зависят также от степени и места повреждения. После поражения головного и спинного мозга в яичках наблюдается десквамация и вакуолизация зародышевых клеток, атрофия семенных канальцев, подавление и прекращение сперматогенеза, а также снижение уровня тестостерона в крови. Важное значение придается вегетативной нервной системе, которая влияет не только на потенцию, но и на сперматогенез.
Врожденные и генетические причины мужского бесплодия
В последние десятилетия отмечается значительный рост количества врожденных патологических изменений яичек, которые достигли в настоящее время 4—5%. Врожденные и хромосомные аномалии развития половых органов, приводящие к бесплодию у мужчин, описаны в соответствующих разделах монографии (крипторхизм, монорхизм, анорхизм, дисгенезия половых желез и др.).
Генетические причины бесплодия могут быть выявлены при соответствующем цитогенетическом обследовании
Инфекционный фактор мужского бесплодия
Важная роль в причинах бесплодия отводится таким заболеваниям, как эпидемический паротит (свинка), сыпной, брюшной тифы, малярия, туберкулез, бруцеллез, венерические заболевания и пр. Частота бесплодия у мужчин после перенесенных инфекционных болезней колеблется, по данным разных авторов, от 8,5 до 36%.
Особое место в мужском бесплодии занимает эпидемический паротит (свинка), который нередко осложняется орхитом. Это осложнение развивается в ходе самого заболевания. При этом поражаются все ткани яичка. Но особо выраженным нарушениям подвергаются его паренхима и семявыносящие канальцы, соединяющие яичко с головкой придатка.
Орхитами, хотя и реже, осложняются и другие инфекционные заболевания (брюшной тиф, паратиф, бруцеллез, грипп, сепсис и др.). Особенно вредным оказывается токсическое влияние на сперматогенный эпителий в случае перенесения нескольких тяжелых инфекционных заболеваний или хронических инфекций. При этом важная роль в патогенезе бесплодия отводится повреждению гематоорхического барьера и развитию аутоиммунного асперматогенеза.
Экзогенные интоксикации и мужское бесплодие
Хронические и острые интоксикации могут оказывать как прямое (первичное) воздействие на генеративную ткань яичка, так и непрямое (вторичное) — вследствие нарушения барьерной функции печени, а также вредного воздействия на нервную Систему. Яды могут вызывать также клеточную гипоксию вследствие конкурентного вытеснения кислорода в молекуле гемоглобина и вследствие токсического поражения эритроцитов. Не меньшее значение, вероятно, имеет и тканевая гипоксия, тесно связанная с метаболическим ацидозом и прямым угнетающим влиянием токсичных веществ на дыхательные ферменты.
Ряд профессиональных и других интоксикаций оказывают вредное действие на зародышевый эпителий яичка. Поэтому рекомендуется особое внимание придавать условиям работы мужчин, имеющих контакт с промышленными ядами, такими как свинец, ртуть, марганец, фосфор, сероуглерод, этиленамин, аммиак, бензол, гранозан, органические перекиси и др. Постоянная работа с этими веществами постепенно может привести к поражению весьма чувствительного герминативного эпителия яичек.
Привычные интоксикации (алкоголь, никотин) и мужское бесплодие
В практическом отношении важное значение имеет злоупотребление алкоголем и табаком. У лиц, страдающих алкоголизмом, определяются выраженные изменения эякулята, которые сводятся к увеличению неподвижных и патологических форм сперматозоидов. На основании клинических и экспериментальных исследований у лиц, страдающих хроническим алкоголизмом, наблюдаются жировая дегенерация зародышевого эпителия и разрастание соединительной ткани в яичке.
Большое значение придается повреждающему действию алкоголя на печень, что в конечном итоге приводит к вторичному выпадению функции яичек.
Фактор питания и мужское бесплодие
Важную роль в процессе сперматогенеза играет пищевой фактор. Недостаточное питание, полное или частичное голодание рано приводят к изменениям в яичках. Эти изменения особенно значительны у детей и подростков до периода полового созревания. Особое значение имеют белки, незаменимые аминокислоты (аргинин, триптофан, лизин, метионин, лейцин и др.) и витамины (А, С, D, Е). Уменьшение содержания этих веществ в пище вызывает расстройства потенции, а также генеративной функции, вследствие изменения ряда защитных систем организма, в частности антиоксидантной системы.
Эндокринные нарушения и мужское бесплодие
Нарушения функции эндокринных и других внутренних органов (щитовидной железы, надпочечников, эпифиза, поджелудочной железы), а также заболевания гипофиза и других желез внутренней секреции также вызывают изменения функции яичек. Эти изменения при невыраженности симптомов, основного заболевания, как правило, не достигают степени азооспермии, а при выраженности эндокринных заболеваний вопрос обычно ставится не о восстановлении плодовитости, а о лечении основного заболевания под наблюдением эндокринолога.
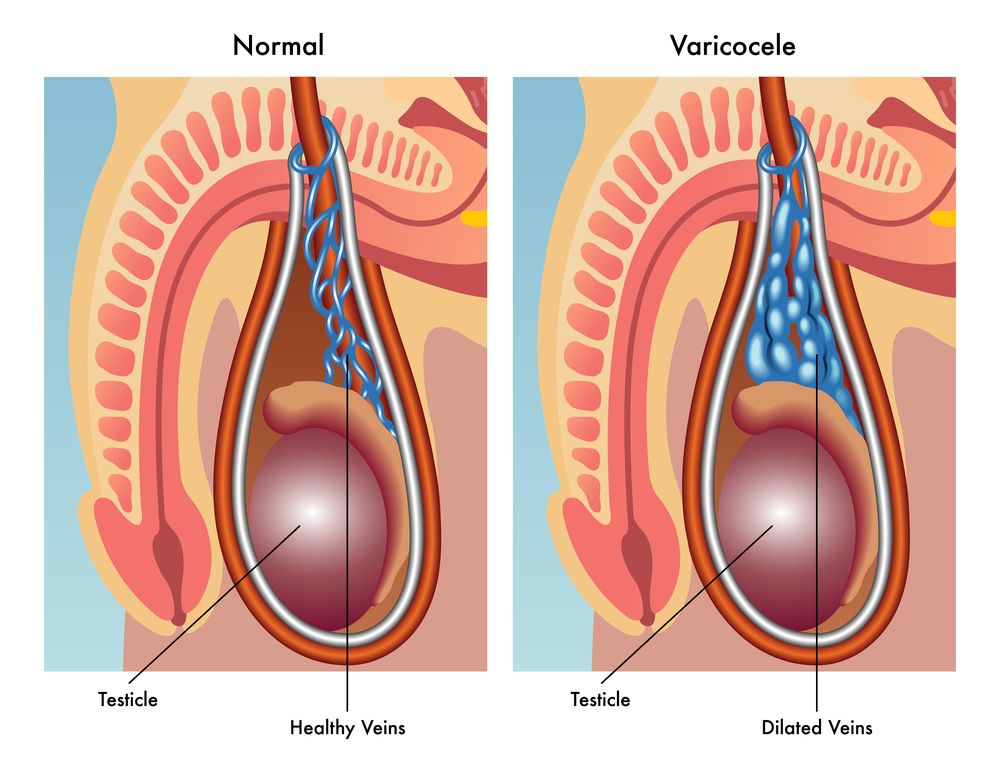
Застой венозной крови в половых органах
Веностаз в половых органах, который развивается вследствие аномалий строения мочеполового венозного сплетения, застойного простатита и других заболеваний, может приводить к гипоксии, нарушению тканевого дыхания, к изменению физиологической функции яичек и придаточных половых желез с развитием бесплодия.
Аутоиммунные поражения половых желез
Важное значение при травме, ишемии, воспалении, воздействии токсичных веществ, а также при температурных влияниях придают нарушению гематоорхического барьера. Этим можно объяснить нарушения сперматогенеза в непораженном яичке при патологическом процессе в контралатеральном.
Нарушение гематоорхического барьера. Накапливается все больше факторов, указывающих на важную роль аутоиммунных процессов в патогенезе асперматогенеза.
Травмы половых органов в зависимости от характера и силы могут привести к необратимым изменениям в структуре и функции яичек.
Операции на оболочках яичка и семенном канатике могут отрицательно влиять на паренхиму яичка и нарушать образование сперматозоидов. Эти нарушения в большинстве случаев необратимы и заканчиваются атрофией семенных канальцев.
У 2% обследованных по поводу бесплодия больных возможной причиной заболевания являются перенесенные в прошлом грыжесечения. К частичной или тотальной стерилизации может приводить травма, возможная при операциях по поводу грыжи, когда в отдельных случаях происходит сжатие сосудов, питающих яички, или же случайная перевязка сосудов и семявыносящих протоков. Придают значение венозному застою, который может наступить после грыжесечения, за счет сдавления семенного канатика тугими швами или наступающим в паховом кольце рубцеванием, что приводит к перерождению ткани яичек и их атрофии.
Патогенез и классификация мужского бесплодия
Согласно современным представлениям, для определения характера лечебных мероприятий при мужском бесплодии следует выделять следующие основные формы: секреторную, экскреторную, аутоиммунную, сочетанную и относительную. Секреторное бесплодие обусловлено гипогонадизмом – недостатоком уровня мужских половых гормонов.
Различают первичный (врожденный) и вторичный (приобретенный) гипогонадизм.
При первичной функциональной недостаточности яичек патологический процесс поражает непосредственно яички (врожденные дисгенезии, крипторхизм, орхит, травмы).
При вторичном гипогонадизме функция яичек страдает в результате поражения гипоталамо-гипофизарной системы, эндокринных и других органов.
Вторичный гипогонадизм, возникающий при различных патологических процессах в гипоталамо-гипофизарной области (травма, стресс, нейроинфекция, опухоли гипофиза и др.), обусловлен резким снижением секреции гонадотропных гормонов, являющихся мощным специфическим стимулятором функции яичек, поэтому вторичный гипогонадизм носит название вторичного гипогонадотропного гипогонадизма.
Большинство исследователей относят поражение яичек вследствие заболевания эндокринных желез ко вторичному гипогонадизму.
Гипосперматогенез клинически проявляется различными степенями олиго-азооспермии. Если патологическое воздействие продолжается, то наступает остановка сперматогенеза на стадии сперматоцитов или сперматогоний, что соответствует азооспермии. При атрофии сперматогенного эпителия (синдром сустентоцитов) в эякуляте выявляется аспермия.
Токсические воспалительные процессы вызывают вакуолизацию и десквамацию глубоких слоев семенных канальцев, их фиброзное перерождение, склероз и атрофию паренхимы яичек. Первичное поражение сперматогенного эпителия сопровождается снижением выработки эстрогеноподобного вещества (ингибина) в сустентоцитах. Выявлена прямая корреляция его содержания в крови с плотностью сперматозоидов в эякуляте.
Экскреторное бесплодие развивается вследствие заболевания или пороков развития мочеиспускательного канала и придаточных половых желез, обструкции семявыносящих протоков, асперматизма. При нормальном сперматогенезе из-за обтурации семявыносящих протоков сперматозоиды и клетки спермиогенеза в эякулят не поступают.
Чем тяжелее процесс, тем значительнее гормональные сдвиги. Снижается уровень тестостерона, возрастает содержание гонадотропинов (ФСГ, ЛГ, ЛТГ) и эстрогенов, что приводит к нарушению сперматогенеза, т. е. развивается секреторное бесплодие.
Двусторонняя непроходимость семявыводящих путей проявляется аспермией – отсутствием сперматозоидов в эякуляте.
Секреторную аспермию от экскреторной при наличии у больного яичек нормальных размеров можно отличить путем гистологического исследования биоптата яичка.
Иммунное бесплодие может быть результатом иммунологического конфликта между супругами (изоиммунное), возникающего, в ответ на поступление в половые пути женщины эякулята, обладающего мощным антигенными свойствами. Конфликту могут способствовать идиосинкразия, несовместимость по системам ABO, HLA, нарушения в состоянии гуморального и центральных звеньев иммунитета и др.
Аутоиммунное бесплодие возникает у мужчин при нарушении гематотестикулярного барьера. Аутоиммунные процессы могут сопутствовать инфекционным заболеваниям, орхитам, травмам яичка, варикоцеле, конгестиям (застою) в мочеполовом венозном сплетении, экзогенным интоксикациям и другим патологическим процессам.
Сочетанная форма бесплодия выделена в 1972. При этом наблюдается сочетание секреторной недостаточности, обусловленной гормональными нарушениями различного характера, и экскреторного компонента в виде воспалительных изменений в добавочных половых железах. Тщательное обследование пациента позволяет решить вопрос, какой из названных факторов превалирует и с чего начинать лечение.
Относительное бесплодие устанавливается в том случае, когда при обследовании супружеской пары патологических изменений не выявляется. Возможно, это связано с несовершенством методов обследования. При относительном бесплодии нередко обнаруживаются иммунологические причины, нарушение функции ЦНС, сексуальные расстройства у женщин, биологическая неполноценность зародышевых клеток; выявляются и другие нарушения.
Диагностика мужского бесплодия
 Брак следует считать бесплодным, если беременность не наступает в течение года нормальной жизни без применения противозачаточных средства.
Брак следует считать бесплодным, если беременность не наступает в течение года нормальной жизни без применения противозачаточных средства.
Диагностика бесплодия у мужчин должна включать анамнез, обследование эякулята, исследование эндокринной функции яичек, надпочечников, гипоталамо-гипофизарной системы, генетическое исследование, при необходимости биопсию яичек.
Особое внимание уделяют заболеваниям половых органов (простатит, везикулит, уретрит, колликулит, эпидидимит), которые отрицательно влияют на генеративную и копулятивную функции. Отмечают состояния, способствующие развитию застойных явлений в органах малого таза (сидячий образ жизни, венная болезнь). Обращают внимание на половое развитие пациента (возраст при первом половом сношении; выраженность либидо, характер эрекции, оргазма, частота половых сношений, их длительность). Важно установить длительность брака, который не сопровождался беременностью жены, наличие детей, родились ли они до заболевания или после него, использование противозачаточных средств.
При дефиците тестостерона наблюдаются слабое развитие мускулатуры, низкая работоспособность, быстрая утомляемость, бессонница, ослабление роста бороды и усов, депрессивное состояние и нарушение половой потенции. Кожа у таких больных нежна и бледна. Холодные руки и ноги указывают на вегетативную лабильность железы и семенных пузырьков.
Исследование эякулята
Решающее значение для диагностики функциональных нарушений половых желез и суждения о плодовитости мужчин имеют макроскопические, микроскопические, биохимические и иммуннологические исследования эякулята. Методы получения эякулята почти всеми исследователями унифицированы. Чаще всего эякулят получают путем мастурбации.
Рекомендуется исследовать эякулят после 4—5-дневного воздержания. Эякулят должен быть получен полностью, так как различные его порции содержат неодинаковое количество сперматозоидов.
Различают следующие изменения эякулята:
Азооспермия характерна для секреторной формы бесплодия, при которой имеется угнетение сперматогенеза на различных стадиях. Это подтверждается нахождением в эякуляте тех или иных клеток сперматогенеза.
Аспермия характерна для экскреторной формы бесплодия и связана с двусторонней обтурацией семявыносящих протоков при нормальной генеративой функции яичек. Однако аспермия может указывать и на полное отсутствие сперматогенного эпителия. Для установления истинной причины патоспермии в таких случаях показана биопсия яичка.
Тератозооспермия характеризуется большим, количеством дегенеративных форм сперматозоидов (менее 4%).
Астенозооспермия — довольно частое патологическое состояние, при ней наблюдается лишь нарушение подвижности сперматозоидов.
Асперматизм — отсутствие выделения эякулята при половом акте. При истинном асперматизме (анэякуляторном синдроме) половой акт не заканчивается семяизвержением, а следовательно, и оргазмом.. При ложном асперматизме половой акт заканчивается семяизвержением и оргазмом, но яэкулят забрасывается в мочевой пузырь.
Иммунологические исследования эякулята. Выявление антител к сперматозоидам. Сперматогенный эпителий хорошо защищен от инфекционных и токсических воздействий гематотестикулярным барьером, который нарушается в исключительных случаях. Повреждение проницаемости или структуры этого гематотестикулярного барьера, образованного собственной оболочкой семенных канальцев и клетками яичка, играет существенную роль в развитии аутоиммунного бесплодия.
Исследование секрета предстательной железы. При микроскопическом исследовании секрета предстательной железы обращают внимание на количество лейкоцитов и лецитиновых зерен в поле зрения. Увеличение количества лейкоцитов (свыше10 в поле зрения) и уменьшение числа лецитиновых зерен характерны для хронического воспаления предстательной железы.
Биопсия яичек. Гистологическое исследование биопата яичек дает возможность определить степень патологического процесса или дегенеративных изменений в нем, способность герминативного эпителия к регенерации и судить о состоянии межуточной ткани, характеризующей эндокринную активность яичек. Она позволяет проводить дифференциальную диагностику между обтурационной и необтурационной формой аспермии и решить вопрос о показаниях к оперативному лечению стерильности. Биопсия показана больным с аспермией и нормально развитыми яичками. Применяется открытая биопсия яичка. Она проводится в амбулаторных условиях с соблюдением всех правил асептики.
Лечение мужского бесплодия
Общие организационные мероприятия. Следует исключить курение, употребление алкоголя, бесконтрольное применение лекарственных препаратов, которые могут сами по себе вызывать нарушение генеративной функции. Необходимо выявить и устранить воздействие вредных профессиональных факторов, так как они нередко могут осложнять положение. Достаточный отдых – сон-период времени, когда организм восстанавливает свои силы, происходит нормализация выработки некоторых гормонов. Но в течение недели важно выделить несколько дней для АДЕКВАТНОЙ физической активности – занятие в спорт зале, плавание, активные виды физической ативности на улице (зимой – лыжи, летом – волейбол, теннис) Однако, физическая активность не должна истощать – оценивайте свое самочувствие после нагрузки – должна быть приятная усталость, возникновение головокружения, тошноты – признаки чрезмерной нагрузки.
Необходимо устранить факторы, вызывающие депрессию, состояние страха, чрезмерные и длительные физические нагрузки. Всем больным следует рекомендовать ежедневное проведение утренней гимнастики, включающей упражнения, улучшающие дыхание, повышающие тонус мыщц тазового дна, брюшного пресса, при малой физической нагрузке необходим активный двигательный режим (ходьба, плавание, подвижные спортивные игры). При физическом характере работы рекомендуется отдых с включением положительных психоэмоциональных нагрузок.
Питание при всех формах бесплодия должно быть регулярным, пища — содержать достаточное количество белков, жиров, углеводов, витаминов, минеральных солей. В пищевой рацион должны быть включены продукты, богатые белками, содержащие незаменимые аминокислоты: мясо животных, птиц, морская рыба, яйца, творог.
Обязательным является употребление растительного масла (подсолнечного, кукурузного, оливкового, арахисового). Необходимо включать в пищу свежие овощи и фрукты (свеклу, морковь, тыкву, абрикосы, яблоки, цитрусовые и др.). Приготовление салатов на растительном масле способствует усвоению жирорастворимых витаминов (A, D, Е, К). Высушенные фрукты служат поставщиками минеральным солей и микроэлементов. Людям с пониженным питанием рекомендуется употребление меда, который содержит витамины, биологически активные вещества, микроэлементы. Запрещается употребление чрезмерно острых блюд, приправ, копченостей.
При установлении режима половой жизни следует учитывать следующие факторы. Частые половые контакты приводят к ухудшению оплодотворяющей способности эякулята за счет уменьшения количества и появления молодых форм сперматозоидов. Редкие половые сношения приводят к увеличению количества сперматозоидов, но способствуют их старению, что также ухудшает оплодотворяющую способность эякулята. 3—5 дневное воздержание является оптимальным сроком для нормализации спермограммы у здорового мужчины. Следует также учитывать дни овуляции у женщин, так как лишь в этот период возможно зачатие. После полового акта жена должна оставаться в постели с приподнятым тазом в течение 30—40 мин, что способствует сохранению семенной лужицы у шейки матки.
Общие лечебные мероприятия. Важное значение для нормализации синтеза половых гормонов, генеративой функции яичек имеет рациональная витаминотерапия. Назначают витамины А, Е, D, К, В1, В2 Имеются комбинированные препараты: витамин А с витамином Е в виде аевитал препараты, содержащие комплекс необходимых витаминов, а также витаминов и микроэлементов, аминокислоты.
Вторичный гипогонадизм. Лечение вторичного (гипогонадотропного) гипогонадизма заключается в применении гонадотропинов, гонадолиберина или препаратов, стимулирующих их выделение. В этом случае показано применение хорионического гонадотропина и его аналогов (хориогонина, прегнила, профази, и др.).
Поэтому введение его можно сочетать с введением андрогенов надпочечникового происхождения, обладающих анаболическим свойством, или чередовать с назначением препаратов, содержащих тестостерон. При отсутствии резервной андрогенной функции яичек лечение хорионическим гонадотропином не имеет смысла. В таком случае следует проводить заместительную терапию тестостероном и другими андрогенами.
При дефиците ФСГ применяют менопаузальный гонадотропин, фолистиман, антрогон. Они содержат преимущественно ФСГ, активирующий сперматогенез. Воздействуя на митотическую стадию сперматогенеза, ФСГ способствует увеличению количества семенных клеток и стимулирует их деление до сперматоцитов. Можно сочетать, назначение фолликулостимулирующего и лютеинезирующего гонадотропинов.
Стимуляторы сперматогенеза – довольно широко распространены. Наиболее часто, в составе комплексного лечения, назначают Спеман, Спеман-форте. Длительность такого лечения составляет не менее 3-6 месяцев.